

L’équité en santé est une préoccupation sociétale majeure dans le monde, les disparités ayant de nombreuses causes, notamment des limitations d’accès aux soins de santé, des différences de traitement clinique et même des différences fondamentales dans les technologies de diagnostic. En dermatologie, par exemple, les résultats du cancer de la peau sont plus mauvais pour les minorités, les personnes à faible statut socio-économique ou celles ayant un accès limité aux soins de santé. Bien que les progrès récents de l’apprentissage automatique (ML) et de l’intelligence artificielle (IA) soient très prometteurs pour améliorer les soins de santé, cette transition de la recherche au chevet doit être accompagnée d’une compréhension approfondie de leur impact sur l’équité en santé.
**L’équité en santé : une définition**
Les organisations de santé publique définissent l' »équité en santé » comme l’équité des chances pour chacun d’être aussi en bonne santé que possible. Il est important de noter que l’équité peut être différente de l' »égalité ». Par exemple, les personnes confrontées à des obstacles plus importants pour améliorer leur santé peuvent avoir besoin de plus d’efforts pour bénéficier de cette juste opportunité. De même, l’équité n’est pas la « justice » telle que définie dans la littérature sur l’IA pour la santé. Alors que la justice d’une IA vise souvent à obtenir des performances égales de la technologie d’IA parmi différentes populations de patients, cela ne met pas l’accent sur l’objectif de prioriser les performances par rapport aux disparités de santé préexistantes.
**Un cadre pour l’équité en santé : HEAL**
Dans l’étude « Health Equity Assessment of machine Learning performance (HEAL) : a framework and dermatology AI model case study » publiée dans The Lancet eClinicalMedicine, une méthodologie est proposée pour évaluer quantitativement si les technologies de santé basées sur le ML fonctionnent de manière équitable. En d’autres termes, le modèle ML obtient-il de bons résultats pour ceux qui ont les pires résultats pour la ou les affections que le modèle est censé traiter ? Cet objectif s’appuie sur le principe selon lequel l’équité en santé doit prioriser et mesurer les performances du modèle par rapport aux disparités de santé, qui peuvent être dues à un certain nombre de facteurs, notamment des inégalités structurelles (p. ex. démographiques, sociales, culturelles, politiques, économiques, environnementales et géographiques).
**Le cadre d’équité en santé (HEAL)**
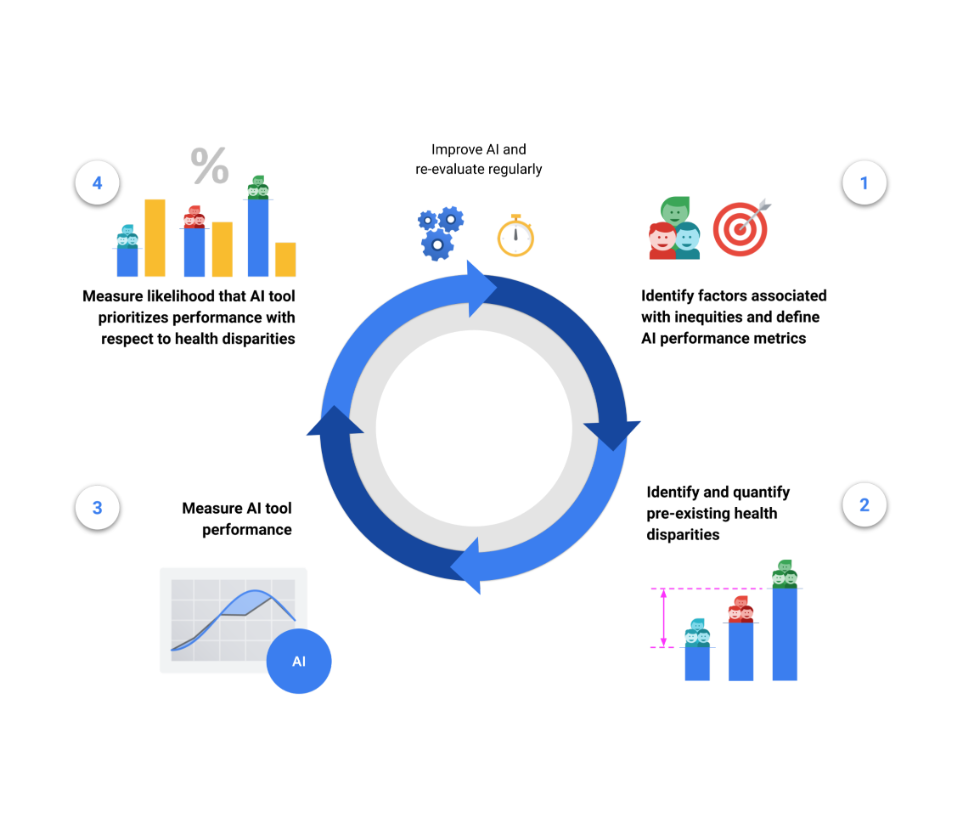
Le cadre HEAL propose un processus en 4 étapes pour estimer la probabilité qu’une technologie de santé basée sur le ML fonctionne de manière équitable :
1. Identifier les facteurs associés aux inégalités en matière de santé et définir les indicateurs de performance des outils.
2. Identifier et quantifier les disparités de santé préexistantes.
3. Mesurer les performances de l’outil pour chaque sous-population.
4. Mesurer la probabilité que l’outil priorise les performances par rapport aux disparités de santé.
Le résultat de la dernière étape est appelé la métrique HEAL, qui quantifie dans quelle mesure les performances du modèle ML sont anticorrélées avec les disparités de santé. En d’autres termes, le modèle fonctionne-t-il mieux avec les populations qui ont les pires résultats pour la santé ?
Ce processus en 4 étapes est conçu pour éclairer les améliorations visant à rendre les performances du modèle ML plus équitables et est censé être itératif et réévalué régulièrement. Par exemple, la disponibilité de données sur les résultats de santé à l’étape (2) peut éclairer le choix des facteurs démographiques et des tranches à l’étape (1), et le cadre peut être appliqué à nouveau avec de nouveaux ensembles de données, modèles et populations.
**Étude de cas sur un modèle dermatologique**
En guise d’étude de cas illustrative, le cadre a été appliqué à un modèle dermatologique, qui utilise un réseau de neurones convolutifs similaire à celui décrit dans des travaux antérieurs. Ce modèle dermatologique d’exemple a été entraîné pour classer 288 affections cutanées à l’aide d’un ensemble de données de développement de 29 000 cas. L’entrée du modèle consiste en trois photos d’un problème de peau ainsi que des informations démographiques et un bref historique médical structuré. La sortie consiste en une liste classée des affections cutanées possibles correspondantes.
À l’aide du cadre HEAL, ce modèle a été évalué en déterminant s’il avait priorisé les performances par rapport aux résultats de santé préexistants. Le modèle a été conçu pour prédire les affections dermatologiques possibles (parmi une liste de centaines) en fonction des photos d’un problème de peau et des métadonnées du patient. L’évaluation du modèle est effectuée à l’aide d’une métrique d’accord des 3 premiers, qui quantifie combien de fois les 3 premières conditions de sortie correspondent à la condition la plus probable suggérée par un groupe de dermatologues. La métrique HEAL est calculée via l’anticorrélation de cet accord des 3 premiers avec les classements des résultats de santé.
Un ensemble de données de 5 420 cas de télédermatologie, enrichi pour la diversité en termes d’âge, de sexe et d’origine raciale/ethnique, a été utilisé pour évaluer rétrospectivement la métrique HEAL du modèle. L’ensemble de données se composait de cas « stockés et transmis » provenant de patients âgés de 20 ans ou plus provenant de fournisseurs de soins primaires aux États-Unis et de cliniques de cancer de la peau en Australie. Sur la base d’une revue de la littérature, la race/l’origine ethnique, le sexe et l’âge ont été choisis comme facteurs potentiels d’iniquité, et des techniques d’échantillonnage ont été utilisées pour garantir que l’ensemble de données d’évaluation comportait une représentation suffisante de tous les groupes de race/ethnie, de sexe et d’âge. Pour quantifier les résultats de santé préexistants pour chaque sous-groupe, des mesures ont été utilisées données publiques approuvées par l’Organisation mondiale de la santé, telles que les années de vie perdues (YLL) et les années de vie ajustées sur l’incapacité (AVCI ; années de vie perdues plus années vécues avec invalidité).
**Conclusion**
Le cadre HEAL permet une évaluation quantitative de la probabilité que les technologies d’IA en santé priorisent les performances par rapport aux disparités de santé. L’étude de cas démontre comment appliquer le cadre dans le domaine dermatologique, indiquant une forte probabilité que les performances du modèle soient priorisées par rapport aux disparités de santé entre les sexes et l’origine raciale/ethnique, mais révélant également le potentiel d’amélioration des affections non cancéreuses dans toutes les tranches d’âge. L’étude de cas illustre également les limites de la capacité à appliquer tous les aspects recommandés du cadre (p. ex., cartographie du contexte sociétal, disponibilité des données), soulignant ainsi la complexité des considérations d’équité en santé des outils basés sur le ML.
Mots-clés : Équité en santé, Apprentissage automatique, Intelligence artificielle, Santé numérique, Cadre HIEL
